- 0546-200-800
- office@otzaracademi.co.il
- מרכז עסקים "לולים" כפר עציון
אנורקסיה נרבוזה כהתנהגות מונעת: הרלוונטיות של חרדה, מתח, פחד ולמידה
Angela S. Guarda ⁎, Colleen C. Schreyer, Gretha J. Boersma, Kellie L. Tamashiro, Timothy H. Moran
עיקרי הדברים
מידע על המאמר
היסטוריה:
התקבל ב 13 למרץ, 2015
אושר ב 2 לאפריל, 2015
זמין באופן מקוון החל מ 3 אפריל, 2015
ביטויי מפתח: אנורקסיה נרבוזה, חרדה, התניית פחד, רכישת הרגלים, אסטרוגן, אנורקסיה מבוססת פעילות
תקציר
התחלואה הגבוהה שקיימת באנורקסיה נרבוזה (AN) והפרעות חרדה מזוהה היטב. אנורקסיה נרבוזה היא הפרעת התנהגות שבה היווצרות של הרגלים מסוימים עשויה לתרום להתמשכותן של התנהגויות א-נורמליות מבחינת אכילה ו פעילות גופנית. שינויים משניים במעגלי המוח הבסיסיים שמדגישים את הערך של התגמול שמתקבל מצריכת מזון ופעילות גופנית, יחד עם הפרעות רעב נוירואנדוקריניות, וסימני אזהרה הנובעים מרעב ופעילות גופנית מוגזמת, צפויים להיות תורמים משמעותיים לחיזוקה של התנהגות אנורקטית באנשים פגיעים גנטית. העניין הוא התפקיד הפוטנציאלי של התניית הפחד במניעת התפתחותה של AN, או הכחדת פחד לקויה תורמים לשיעור הגבוה של ההופעה מחדש שנצפתה לאחר שיחזור המשקל. ראיות ממודלים של חרדה שמבוססים על בעלי חיים ומחקרים אנושיים מעידים על כך שאסטרוגן נמוך פוגע בהכחדה. רמות נמוכות של אסטרדיול ב-AN עשויות אפוא לשחק תפקיד בהנצחת הפחד ממזון ושומן בקרב חולים שעברו שיחזור משקל לאחרונה. מודלים של תרגום בכללם מודל הפעילות מבוסס אנורקסיה (ABA) מודל המכרסם של AN, והדמיה נוירולוגית של פחד הכחדה ומיזוג, יכולים לעזור להבהיר את המנגנונים המולקולריים הבסיסיים המעורבים בהתנהגויות של הימנעות ממזון ב-AN. יתר על כן, התאמה של התערבויות טיפוליות בעלות יעילות בהפרעות חרדה עשויות לתרום לפיתוח טיפולים חדשים עבור הפרעה פוגענית זו.
תוכן עניינים
1. מבוא
אנורקסיה נרבוזה (AN) היא הפרעה התנהגותית מורכבת עם אחוזי תחלואה ותמותה גבוהים [1]. היא מאופיינת בהרעבה עצמית, פעילות גופנית מופרזת, הימנעות חולנית מאכילה, ופחד מוגזם מהשמנה, יש לה אופי מוטיבציוני, והיא בעלת דמיון פנומנולוגי להתמכרות [2]. ליקויים ברגולציה של המעגלים הנוירוטיים שבבסיסם של החרדה והתגמול, כמו גם הפרעות מונעות הרעבה בהומוסטאזיס של התיאבון ובאותות השובע, מוטמעות באטיולוגיה של האנורקסיה נרבוזה [3 – 7]. רוב השינויים הפיזיולוגיים הללו קשורים למצב נתון והפיכים; אולם ישנן ראיות הולכות וגוברות שמצביעות על כך שתגובות מוקדמות תורמות להתפתחות והתחזקות של הגבלות על אכילה ופעילות גופנית מוגזמת.
שיעור השכיחות של אנורקסיה נרבוזה מבוסס על הקריטריונים המתוארים במהדורה הרביעית של המדריך האבחוני והסטטיסטי של הפרעות נפשיות (DSM) והוא בסביבות ה- 0.9% [7]. נתון זה עשוי להיות קרוב יותר ל-1.7% עם בוחנים אותו באמצעות קריטריוני האבחון המורחבים של DSM-5 [8]. רוב המקרים מתרחשים בנקבות, כאשר ההערכות התורשתיות מבוססות על מחקרי תאומים שמראים שיעור של 48-88%, וסיכון של פי עשר לקרובי משפחה מדרגה ראשונה של נשואי הבדיקה [9, 10]. לא ידוע כיצד הפגיעות הגנטיות הבסיסית תורמת לאטיולוגיה של האנורקסיה נרבוזה. החלון הצר יחסית של תחילת ההפרעה [7] והמובהקות של הופעת ההפרעה בעיקר בקרב נשים מצביעה על כך שלאסטרוגן יש תפקיד משמעותי בהתפתחות ההפרעה. מחקרי תאומים ובעלי חיים תומכים בכך שאסטרוגן הוא גורם סיכון גנטי בסיסי להפרעות אכילה בגיל ההתבגרות [11]. המכניזם של קשר זה עשוי להתייחס לוויסות האסטרוגן בשעתוק גנים בתוך מערכות הנוירוטרנסמיטר הרלוונטית לתגמולי מזון, פגיעות מלחץ או חרדה והוא עשוי להיות שונה במקרים חדשים או בהתפרצות כרונית. חרדה היא תכונה המשויכת לגורמי הסיכון שעלולים להוביל להתפתחות של הפרעות אכילה [12], לנטייה מוקדמת להתפתחות הפרעות חרדה [13] ולליקוים בהתניית פחד, הכחדת פחד או למידת בטיחות [14 – 17]. התניית פחד לקויה בתורה, הוצעה כמנגנון פוטנציאלי שמסביר את ההתפתחות המהירה והמתמדת של הגבלות על צריכת קלוריות ופחד מהשמנה [18].
למרות התחלואה הגבוהה והתמותה, הטיפולים היעילים הקיימים כיום מוגבלים, כאשר הראיות הטובות ביותר מגיעות מתחום הטיפול המשפחתי למתבגרים עם אנורקסיה נרבוזה [19, 20]. הפרוגנוזה טובה יותר בקבוצת גיל זו, היא סביר להניח מכיוון שיש אחוז גבוה יותר של מקרים מתונים מבחינת הגבלה עצמית, עם נטייה גנטית חלשה יותר ומשך מחלה קצר. להשוואה, בקרב מבוגרים עם אנורקסיה נרבוזה כרונית, אין ניסוי אקראי מבוקר למציאת טיפול שהוכיח יעילות בהשגת הפוגה, למרות זאת, יש קונצנזוס בין המומחים שתומך בשיטות התנהגותיות מבוססת בית החולים שיחזור משקל במידת הצורך, אם לא מספיק עבור התאוששות [21, 22 ]. נתוני קורלציות מצביעים בחוזקה על כך ששחרור מבית החולים עם BMI גבוה לאחר שיחזור משקל בגישות התנהגות מבוססות בית חולים מראה על שיעור נמוך יותר של נסיגה והופעה מחדש של ההפרעה [23 – 26]. למרות שטיפול באשפוז יכול להיות מציל חיים, הוא יקר וקשה להשגה [27]. יתר על כן, שיעורי הנסיגה לאחר שישה חודשים באשפוז ושיחזור משקל קרובים ל- 50% [28, 29]. לאחר שבוססו, קשה להכחיד דפוסי אכילה מגבילים והם נוטים להימשך בהתמדה [30], ומגוון תזונתי מוגבל בקרב חולים לאחר שיחזור משקל נמצא כגורם מנבא להתדרדרות שנה לאחר האשפוז [31]. באופן מפתיע, עם זאת, ישנם מעט מחקרים שבוחנים התערבויות ממוקדות במניעת נסיגה בשחזור המשקל הבא.
סקירה זו תתמקד בקשר בין חרדה לבין אנורקסיה נרבוזה כולל מנגנונים פוטנציאליים שבהם חרדה, מתח ולמידת פחד תורמים לאטיולוגיה ולתחזוקה של הפרעה זו וכיצד אסטרוגן יכול להשפיע על האסוציאציות הללו (איור 1). בסקירה תינקט גישה תרגומית שתתבסס על עבודה שנעשתה במודלים בעלי חיים ודימות מוחי במטרה להעביר מידע לחוקרים עתידיים בנוגע לפסיכופתולוגיה של האנורקסיה נרבוזה והתחזוקה שלה, והפוטנציאל לפיתוח של טיפולים משופרים עבור מצב זה.
2. תחלואה וחפיפה פנומנולוגית בין אנורקסיה נרבוזה וחרדה
תחלואה גבוהה של אנורקסיה נרבוזה עם הפרעות חרדה, מוכרת היטב ומקושרת לחומרת המחלה כולל BMI נמוך [32] והפרעות אכילה חזקות יותר בפסיכופתולוגיה [33, 34]. הפרעות החרדה הנפוצות ביותר בתחלואה עם הפרעה טורדנית-כפייתית (OCD) והפרעות חרדה חברתית (SAD) [34]. הפרעות חרדה חברתית חולקות בנוסף את העיסוק באופן שבו אדם נתפס על ידי אחרים כתכונה מרכזית [35]. תכונות אישיות חרדתיות, כולל נוירוטיות מוגברות, פרפקציוניזם והימנעות מפגיעה, כמו גם ירידה בחדשנות מאובחנות לעתים קרובות בהפרעה טורדנית-כפייתית, הפרעות חרדה ואנורקסיה נרבוזה [12, 13] ועשוית להצביע על מסלול משותף לפיתוח של הפרעות חרדה ואנורקסיה נרבוזה. באנורקסיה נרבוזה תכונות אישיות, חרדה, פרפקציוניסטית ואובססיביות, נוטות להיות תורשתיות [32, 36], מראות על החמרה בהרעבה [37 – 39], נמשכות לאחר ההחלמה [4, 40 – 42] ומנבאות פרוגנוזה עגומה [43].
אנורקסיה נרבוזה בדרך כלל מתחילה בהתבגרות, עם ההחלטה להתחיל דיאטה ולאבד כמה קילוגרמים או בעקבות אובדן משקל ראשוני בלתי רצוני המיוחס למחלה ארעית או גורם לחץ פסיכו-סוציאלי. הגבלת קלוריות מתפתחת באופן מצער להתנהגות נמנעת שמקושרת עם קוצר נשימה, חרדה מארוחות, והתנהגויות נמנעות כאשר מתמודדים עם צריכת מאכלים עתירי קלוריות. משטרים של אכילה ופעילות גופנית נעשים נוקשים, הרפרטואר התנהגותי מוגבל, ויש ליקוי פונקציונלי מתקדם. בשתי הפרעות החרדה, החששות מאורגנות סביב אמונה לא רציונלית הקשורה לדריכות מוגברת ולחרדה מובהקת. בניגוד להפרעות החרדה ביותר עם זאת, לאנורקסיה נרבוזה יש גם איכויות אגוסינטוניות ומתגמלות, מה שגורם לאמביוולנטיות כלפי טיפולים שמיועדים דיאטה או התנהגויות תרגיל [44].
3. למידה, היווצרות הרגלים, מתח והתניית פחד: רלוונטיות לאנורקסיה נרבוזה
מרבית העניין לאחרונה מתמקד בתפקיד שיש להיווצרות הרגלים בתרומה לחיזוק ההתמדה של התנהגויות שמשויכות לאנורקסיה נרבוזה ומתקדמות לקראת השלכות שליליות יותר ויותר [30]. לפי תפיסה זו, באנורקסיה נרבוזה דיאטה ופעילות גופנית מתחילות כהתנהגויות מכוונות מטרה, שמבוססות על למידה אינסטרומנטלית, ומונעות על ידי הרצון להגיע לתוצאה הרצויה של ירידה במשקל. עם זאת, לאורך זמן התנהגויות אלה נהפכות בהדרגה לגירוי כפייתי – תגובה או דפוס התנהגות, ללא התחשבות בהשלכות שליליות, קבועות יותר ויותר ואוטומטיות, ומכוונות על ידי גורמים סביבתיים וסימנים אינטרוספקטיביים. התקדמות זו דומה לזו המתוארת בשימוש בחומרים ממכרים; כאשר בתחילה המשתמש בחומר בוחר לעשות זאת מתוך רצון נהנתני, לאורך זמן השימוש נהפך לתבנית התנהגותית כפייתית ובלתי מבוקרת [45, 46]. במישור העצבי, המעבר לפעולה מבוססת גירוי-תגובה מלווה במעבר משליטה קדם-מנטלית לשליטה סטרלית בהתנהגות, התנהגות וממעורבות ונטרלית למעורבות דורסל סטרלית [45, 47].
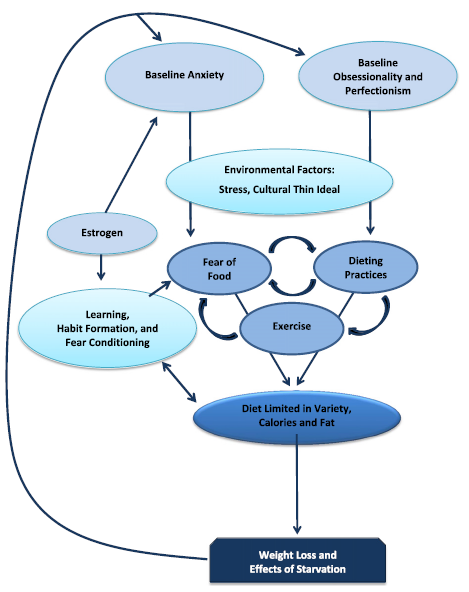
איור 1. מודל סכמתי של גורמים המשפיעים על פיתוח ותחזוקה של אנורקסיה נרבוזה (מתאים למודל המוצע על ידי שטיינגלאס ושות’ , 2011). תכונות אישיות כמו חרדה מורבידית ואובססיביות מגבירות את הפגיעות לאנורקסיה נרבוזה ומחריפות את הירידה במשקל. ישנה עליה באסטרוגן בתחילתן של הפרעות אכילה וגם בהפרעות חרדה ונמצאו ברמות גבוהות אצל נקבות. הטריגרים להתפרצותה של אנורקסיה נרבוזה מופעלים על ידי חשיפה לגורמים סביבתיים כולל מתח ולחץ סוציו-תרבותי לעשות דיאטה, מה שמוביל למעגל של הסלמה בדיאטה, פעילות גופנית וחרדה בנוגע לאכילה מחוזקות על ידי למידה, היווצרות הרגלים והתניית פחד. לאחר שהפרעה נהפכת לכרונית, ההשפעות של הרעב ורמות אסטרוגן נמוכות עלולות להשפיע על הלמידה והכחדת הפחד ובכך לתרום הן להמשכיות של הפחד מאוכל במהלך השלבים המוקדמים של שיחזור המשקל וגורמות לשיעורי התדרדרות גבוהים.
מחקרים ניסיוניים בהתניית פחד והכחדת פחד שנערכו במודלים של בעלי חיים ובדימות מוחי בבני אדם, עזרו להבהיר את המעגלים העצביים בבסיס הפחד. האמיגדלה, אזור במוח עם רמה גבוהה של קולטנים מסוג גלוקוקורטיקואיד [55], הוא גורם מרכזי בהתניית פחד והוא מופעל בעקביות הן על ידי גירויים מותנים וגירויים בלתי מותנים, בעוד שקליפת המוח הפרונטלית (vmPFC) ממלאת תפקיד חשוב בהכחדה מלמעלה למטה של למידת פחד דרך ההקרנות הקורטיקולימביות לאמיגדלה [56, 57]. התניית פחד הוי התהליך שבו גירוי מותנה (CS), מקושרת שוב ושוב עם גירוי בלתי מותנה (US), מה שגורם לתגובת הפחד להתעורר באופן עצמאי. לעומת זאת, הכחדת הפחד היא תהליך למידה שהגירוי המותנה כעת בטוח, ומציג אותה שוב ושוב ללא גירוי לא מותנה עד שתגובת הפחד המותנית נכחדת.
האמונה הרווחת היא שהתניית פחד והכחדת פחד הן תהליכי למידה מובהקים המושפעים על ידי גורמים גנטיים ותרופתיים שונים אשר משפיעים על הפלסטיות העצבית [58, 59]. התניית פחד תוארה כקלה ללמידה אבל קשה לזכירה, כאשר פחדים שהוכחדו מופעלים בקלות ועלולים להופיע מחדש כשמתרחשים שינויים סביבתיים, קונטקסטואליים, או במצב הפנימי [60]. פחד לקוי מפני הכחדה ורגישות להתניית פחד צפויים להיות רלוונטיות לאנורקסיה נרבוזה, כאשר המטופלים מתקשים לטפל בפחד שלהם ממזונות עתירי קלוריות גם לאחר חשיפה מבוססת-בית-חולים לצריכת מאכלים אלה, וממשיכים להתלונן על חוסר שביעות רצון ממבנה הגוף גם כמה חודשים לאחר שיקום המשקל. יתר על כן, למרות שישנן כמה ראיות מעורבות, בקרב אנשים עם תכונות של חרדה גבוהה או הפרעות חרדה, הפחדים המותנים מופיעים מחדש בקלות יתרה, הכחדת הפחד מעוכבת, ו/או ישנן לקוית בשימור של למידת ההכחדה [14, 15, 60 – 65].
למרות שמודלים של בעלי חיים של אנורקסיה נרבוזה הם לא מושלמים ולא מחקים היבטים פסיכולוגיים של הפרעת, הפעילות מבוססי אנורקסיה (ABA) מודל המכרסם של לוכד שני מאפיינים התנהגותיים קריטיים של אנורקסיה נרבוזה, פעילות גופנית מוגזמת והסלמה בהגבלות על האכילה עד לכדי הרעבה [66 – 68]. מודל ה-ABA ממחיש כי בקביעת הגבלות על האכילה, פעילות גופנית יכולה להיות מונעת ומתגמלת בבעלי חיים, ללא תלות בנימוקים קוגניטיביים כגון פחד מהשמנה [67]. בפרדיגמה זו, כאשר גישה לאוכל מוגבלת בנוכחות של גלגל ריצה, בעלי החיים באופן פרדוקסאלי מגבירים את האינטנסיביות של הפעילות הגופנית שלהם, צורכים פחות אוכל מאשר בישיבה, מאבדים יותר משקל, ומריצים את עצמם למוות בתוך כמה שבועות. ישנה פגיעות אישית ברגישות ל-ABA, אבל נקבות חולדה צעירות עם רמות פעילות גבוהות יותר בקו היסוד נוטות לאכול פחות, לרוץ יותר, ולאבד את המשקל הגדול ביותר [68 – 70], בעקביות עם האבחנה הקלינית באנורקסיה נרבוזה לעתים קרובות פעילות גופנית מוגזמת מקדימה לדיאטה והסלמה בהרזיה [71, 72]. פעילות גופנית מוגזמת הוכרה מזה זמן רב כסימן ההיכר של אנורקסיה נרבוזה [73], היא מופיעה בעד 80% מהמקרים ובעלת תפקיד מרכזי בפתוגנזה של התקדמות של ההפרעה [74]. יתרה מזאת, פעילות גופנית מוגזמת מקושרת עם שיעורי הופעה מחדש גבוהים לאחר שיקום משקל [25, 28, 75] ועם נטיות אישיותיות לאובססיה וחרדה [74, 76, 77].
פעילות גופנית הוצעה כממלאת תפקיד של נוגד חרדה באנורקסיה נרבוזה והיא מקושרת לעמידות ללחץ בבעלי חיים [78]. למרות שהאפקט הזה יכול להחזיק בתחילת ההתפתחות של האנורקסיה נברוזה, כאשר המשקל עדיין בגדר הנורמלי, החרדה בדרך כלל מחמירה עם ירידה במשקל ומשתפרת עם שחזור משקל [75], כך שכל השפעה זמנית נוגדת חרדה של פעילות גופנית צפויה להתערער על ידי ההשפעות מזיקות של הרעבה עצמית על לחץ וחרדה כמו ירידה מואצת במשקל. אכן, באנורקסיה נרבוזה חריפה, הפעילות המוטורית הייתה בקורלציה עם רמות גבוהות יותר של קורטיזול בשתן במשך 24 שעות ביממה [79]. באופן דומה, קוריקסטרון פלזמה, הגלוקוקורטיקואיד העיקרי במכרסמים, גבוה בקרב בעלי חיים שעברו את פרוטוקול ABA [80]. היסטוריה של חשיפה ל- ABA במהלך גיל ההתבגרות הוכחה כבעלת השפעות ארוכת טווח על התנהגויות חרדתיות כמו מדד נוירואנודקורין של פעילות בציר HPA בנקבות חולדה בוגרות שחזרו למשקל גוף נורמלי [66]. בבעלי חיים אלה עליה מתמדת בקוריקסטרון פלזמה ושחרור מוגבר של הורמון קורטיזול (CRH) mRNA בגרעין הפאראוונטריקולרי והאמיגדלה לאחר חשיפה ללחץ אקוטי.
שינויים ברעב ואותות השובע, בדומה לאלה שנצפו אצל נשים עם אנורקסיה נרבוזה [5], נמצאו במכרסמים החשופים ל-ABA וכוללים רמות לפטין ירידה. רמת לפטין נמוכה ממלאת תפקיד מרכזי בהרעבה עצמית כולל היפראקטיביות. תוספי לפטין אקסוגניים מאשרים שיש קשר בין ה- ABA לשינויים ב-HPA ובציר HPA [81]. יתר על כן הזרקה של לפטין לטגמנטום הונטרלי של חולדות ABA מפחית את השימוש בגלגל ריצה; אפקט שהוצע כי מתייחס להשפעה של לפטין על אותות הגחון הטאסנטלי [82]. הנחה זו, כי הרעבה עצמית כולל היפראקטיביות מביאה לניתוק באותות התגמול, תואמת את האבחנה הקלינית כי אנשים עם אנורקסיה נרבוזה מתארים פעילות גופנית כמתגמלת. בהתאם להשקפה זו, הפרדיגמה האחרונה של fMRI ודימות וקיבעון במבט הראתה כי גירויים חזותיים שמקושרים לפעילות גופנית מוגברת של הסטריאטום הגחוני באנורקסיה נרבוזה לעומת קבוצת בקרה של נשים [83].
הוכח בנוסף כי לפטין מסייע בהכחדה של הפחד וישנם מאפיינים של נוגדי חרדה בחולדות [84, 85]. למרות שהמנגנון המולקולרי אינו ברור, לפטין מגביר את התפקוד של חומצת N-methyl-D-aspartic בקולטן, כמו גם חיזוק ההיפוקמפוס בטווח הארוך וידוע כי ממלא תפקיד למידה וזיכרון [81]. באופן מעניין, החשיפה ל-ABA במכרסמים מחזק את אפקט הסלידה מטעם (סוכרוז) בשילוב עם גירוי רעיל הגורם בחילות (הזרקת ליתיום כלוריד לצפק). יתרה מזאת, התוצאה של ABA היא השהיית ההכחדה של שנאת מזון מותנית זו לאחר שהסוכרוז כבר אינו משולב עם ליתיום כלוריד [86]. מכיוון שהפרעות במערכת העיכול ממלאות תפקודית ראשי באנורקסיה נרבוזה [87], פחד מפני אי נוחות בעיכול בעקבות צריכת מזון צפוף עתיר קלוריות עשוי לתרום להימנעות מתמשכת ממאכלים אלה בקרב חולי אנורקסיה נרבוזה שסיימו לאחרונה שיחזור משקל, בעוד שהסיכון לנסיגה גובר. מנגנון זה עשוי גם להנציח הימנעות מזון במקרים חריגים של אנורקסיה נרבוזה שבהם לא מתקיים פחד מהשמנה והוא עקבי עם תוצאות מחקרי fMRI האחרונים שמקשרים בין כאבי בטן להתניית פחד והכחדת פחד בקרב אנשים עם תסמונת המעי הרגיז [88].
5. אסטרוגן, חרדה ופחד מאוכל ושומן באנורקסיה נרבוזה
האסטרוגן עלול להשפיע הן על הסיכון בהתפרצות של האנורקסיה נרבוזה והן על התחזוקה שלה באמצעות מגוון רחב של מנגנונים. השפעת האסטרוגן על צריכת המזון מוכרת היטב, ובאופן כללי, אסטרדיול נמוך מקושר לצריכת מזון גבוה יותר במהלך גיל המעבר בעלי חיים כרותי שחלות [89]. למרות שהשפעה זו על צריכת המזון עשוי להיראות קשה ליישוב עם רמת האסטרוגן הנמוכה של אנורקסיה נרבוזה אקוטית, נתונים חדשים על ההשפעות של אסטרוגן על חרדה ולמידה עשויים לתרום לתחזוקת התנהגויות אנורקטיות באנשים החולים באנורקסיה נרבוזה. נשים עם אנורקסיה נרבוזה ואוליגומנוריאה או אמנוראה דיווחו על רמות גבוהות יותר של פגיעות ללחץ במהלך המחקר האחרון שהשתמש בהערכה אקולוגית [90], ואילו שימוש באסטרדיול שיפר את הניקוד של תכונת החרדה בסולם STAI בניסוי סמיות כפולה של תוספי אסטרוגן לצפיפות העצם אצל מתבגרים עם אנורקסיה נרבוזה[91]. כריתת שחלות אצל עכברים מקושרת עם חרדה מוגברת שבועות לאחר הניתוח, מה שמצביע על כך כי מניעה לטווח ארוך של הורמונים שמיוצרים על ידי השחלות עלולה להגביר את תסמיני החרדה בתגובה ללחץ [92]. הפחד מההאכלה גדול במידה ניכרת בקרב נקבות חולדה לעומת זכרים מה שתומך עוד יותר בכך שלאסטרוגן יש תפקיד בלמידת פחד שמשפיע על התנהגות האכילה [93, 94]
בספרות על חרדה, הנוהל של אסטרדיול הוכח כנוגד חרדה וכמזרז הכחדה של למידה הפחד בבני אדם ומכרסמים [95-97]. אפילו מנה אחת של אסטרדיול, שניתנה בשלב המחזור בו זקיקי האסטרוגן נמוכים באופן טבעי, הביא לשיפור בהכחדה של פחד [95, 96]. רמות אסטרוגן גבוהות יותר הוכחו בנוסף כמעכבות את למידת הפחד אצל נשים עם הפרעת דחק פוסט טראומטית (גם כן הפרעת חרדה) [98]. למרות אסטרדיול פיסיולוגי מגביר את הכחדת הפחד, גלולות למניעת הריון (ocps) אשר ניתנות לעתים קרובות לנשים אמוררייאית עם אנורקסיה נרבוזה, מכילות אתיניל-אסטרדיול. אתיניל-אסטרדיול מדכא אסטרדיול אנדוגני [97, 99] והוכח כי פוגע בהכחדה של פחד בחולדות, השפעה שמתהפכת על ידי קולטני אסטרוגן אגוניסט. גלולות למניעת הריון ( (OCPs מקושרות גם עם ליקויים בהכחדת פחד בפרדיגמת ניסויים ניסיונית בנשים בריאות [96,100].
באנורקסיה נרבוזה כרונית,, אסטרוגן נמוך הנובע מהיפוגונדיזם אמנוראה, עשוי לסייע לשמר על הפחד מפני מזון, פוביה מהשמנה, וחרדה מוגברת. במהלך השלבים המוקדמים של שחזור משקל, כאשר רמות האסטרוגן נשארת תת-פיזיולוגית, רמת האסטרוגן הנמוכה עשויה לתרום לנסיגה לאחר טיפול בבית החולים וייתכן שתוספי אסטרדיול עשויים להיות בעלי ערך תרפויטי וראויים למחקר נוסף אודותיהם.
6. ההשלכות על הטיפול
טיפול מוצלח בהתמכרות כרוך במניעה של תוצאות מתגמלת והימנעות משימוש פוגעני בסמים, ואילו בטיפול בהפרעות חרדה טיפול מוצלח דורש הסרת תוצאות שליליות והכחדת פחד. טיפול מוצלח באנורקסיה נרבוזה דורש הפסקה של פעילות גופנית מוגזמת ושל ההגבלות התזונתיות, כמו גם הכחדה של החרדה המוגברת והתנהגויות של הימנעות מארוחות המאפיינות את ההפרעה. ואכן, חרדה לפני הארוחה נמצאה הפיכה בהקשר של צריכת מזון בארוחה סטנדרטית אצל אנשים עם אנורקסיה נרבוזה[101].
למרות שחשיפה עם מניעת התגובה (ERP) היא התערבות יעילה ביותר להפרעות חרדה, מחקרים הבוחנים את היישום שלה באנורקסיה נרבוזה הוזנחו יחסית [102]. למרות זאת, אלמנטים של ERP מוטמעים בפרוטוקולים התנהגותיים מבוססי בית החולים ובטכניקות של הכשרה הורית בטיפול משפחתי לאנורקסיה נרבוזה [103-106]. הגברת תשומת הלב לטיפול בפחדים ממגוון מזונות מסוכנים במספר רב של אירועים חברתיים המבוססים על ארוחות, עשויה להיות חשובה כדי שיהיה ניתן להכליל הכחדה של פחד לצריכת מזון בקלוריות גבוהה, ולמזער את הנסיגה לאחר טיפול מבוסס בית חולים. טיפול בדימוי הגוף לאחר שחזור המשקל צפוי גם הוא להיות בעל חשיבות, למרות שהתערבויות שמתמקדות בנרמול דימוי הגוף במהלך העלייה במשקל הינן בעלות סבירות פחותה להיות יעילות. השימוש בסביבות מציאות וירטואלית עשוי לספק כלי חדשני להכשרת הכחדה [107].
מספר סוכנים נראים מבטיחים כתוספים להתערבות ERP בהפרעות חרדה. אלה כוללים ציקלוסרין (D), ומשפר קוגניטיבי NMDA אגוניסט חלקי, שמשמשים כדי לחזק את הכחדת הפחד [108], פרופראנולול שמחליש את זיכרון הפחד; ומספר מעכבי ספיגה חוזרת של סרוטונין [60, 63]. עם זאת, יש מחסור בתוצאות עקביות שחוזרות על עצמן. באנורקסיה נרבוזה מחקר קטן של ציקלוסרין (D) היה גם שלילי [109], כך גם במחקר הפיילוט האחרון של אלפראזולאם אשר לא הראה השפעה על חרדה בהקשר של ארוחות או צריכת מזון [110]. למרות שבנזודיאזפינים הם נוגדי חרדה, הם גם סוכנים של מחלות ופוגעים בקונסולידציה של הזיכרון, מה שעלול לפגוע באפקטיביות שלהם בטיפולים בחשיפה לארוחות. הראיות האחרונות תומך ביעילות אפשרית של קוצב וגאלי (VNS) כגורם מצמצם חרדה בהתערבות טיפולית להפרעות חרדה עמידות [111]. מנתונים שנאספו על בעלי חיים עולה כי VNS מביא להפוגה בהתניית פחד לאחר הכשרת הכחדה, ואפנון הפוטנציאל המתעורר בדרכי הגישה של vmPFC אל האמיגדלה [112,113]. טיפולים חוזרים בגרייה מגנטית של ה- vmPFC היא טכניקה נוירומודולפית נוספת אשר מראה הבטחה בחקר הכחדה של פחד בבעלי חיים ובבני אדם [103,114]. שתי טכניקות אלה עלול להיות בעל יישום כמו התערבויות למניעת התדרדרות עבור אנורקסיה נבוזה.
7. מסקנות
מחקרים שנערכו לאחרונה בתחומי מדעי המוח של הלמידה והתמכרות העשירו את הבנתנו בנוגע לאנורקסיה נרבוזה הפרעת ההתנהגות מונעת. הן הפרעות חרדה והן אופי חרדתי כבר מזמן הוכרו במידה כבעלות קשר הדוק לאנורקסיה נרבוזה, אך רק לאחרונה נערכו מחקרים שבחנו את המנגנונים שבבסיס של מערכת היחסים הזאת. עבודה מנטלית של למידה, התניית פחד, ומודלים של בעלי חיים של יכולים לתרום להבנה חדשה של האטיולוגיה המורכבת והתחזוקה של הפרעה זו. למרות שיש מגבלות ביישום של מודלים של חיות בסיוע שלהם להבנת התנאים הפסיכיאטריים האנושיים, הם נותנים את האפשרות לשחזר היבטים מסוימים של ההפרעה כדי להבהיר מנגנונים פתופסיכולוגיים, כולל שינויים נוירואנדוקרינים ואפיגנטיים שנגרמים על ידי פעילות גופנית מוגזמת, הגבלת מזון, לחץ ואסטרוגן, שעשויים לתרום לסיכון, ותחזוקה של אנורקסיה נרבוזה. מודלים של בעלי חיים עשויים בנוסף לסייע בבדיקת טיפולים תרופתיים או נוירומודולוגיים חדשים, כולל אלה בעלי יעילות מוכחת או מבטיחה בטיפול בהפרעות חרדה. אתגר משמעותי בטיפול בחולי אנורקסיה נרבוזה חמורה וכרונית הוא פיתוח של התערבויות מניעה אפקטיביות שימנעו נסיגה והופעה מחדש בקרב חולים שעברו טיפול שחזור משקל מבוסס בית חולים. טיפולים ממוקדים בחרדה והכחדת פחד בחולים שסיימו לאחרונה שחזור משקל עשויים לפיכך להיות מבטיחים. הכללה מוצלחת של התנהגות אכילה נורמלית ובחירת המזון במצבים חברתיים שונים יכולה להיות חשובה במיוחד בסיוע לחולים כרוניים בהתאוששות מהפרעה חמורה ומתישה זו.
הפניות
1] J. Arcelus, A.J.Mitchell, J.Wales, S. Nielsen, Mortality rates in patientswith anorexia
nervosa and other eating disorders. A meta-analysis of 36 studies, Arch. Gen.
Psychiatry 68 (2011) 724–731.
[2] C. Davis, G. Claridge, The eating disorders as addiction: a psychobiological perspective,
Addict. Behav. 23 (1998) 463–475.
[3] L.M. Holsen, E.A. Lawson, J. Blum, E. Ko, N. Makris, P.K. Fazeli, A. Klibanski, J.M.
Goldstein, Food motivation circuitry hypoactivation related to hedonic and
nonhedonic aspects of hunger and satiety in women with active anorexia nervosa
and weight-restored women with anorexia nervosa, J. Psychiatry Neurosci. 37
(2012) 322–332.
[4] W.H. Kaye, C.E. Wierenga, U.F. Bailer, A.N. Simmons, A. Bischoff-Grethe, Nothing
tastes as good as skinny feels: the neurobiology of anorexia nervosa, Trends
Neurosci. 36 (2013) 110–120.
[5] P. Monteleone, M. Maj, Dysfunctions of leptin, ghrelin, BDNF and
endocannabinoids in eating disorders: beyond the homeostatic control of food intake,
Psychoneuroendocrinology 38 (2013) 312–330.
[6] W. Kaye, Neurobiology of anorexia and bulimia nervosa, Physiol. Behav. 94 (2008)
121–135.
[7] J.I. Hudson, E. Hiripi, H.G. Pope Jr., R.C. Kessler, The prevalence and correlates of eating
disorders in the National Comorbidity Survey Replication, Biol. Psychiatry 61
(2007) 348–358.
[8] F.R. Smink, H.D. van, A.J. Oldehinkel, H.W. Hoek, Prevalence and severity of DSM-5
eating disorders in a community cohort of adolescents, Int. J. Eat. Disord. 47 (2014)
610–619.
[9] A. Hinney, A.L. Volckmar, Genetics of eating disorders, Curr. Psychiatry Rep. 15
(2013) 423.
[10] M. Strober, R. Freeman, C. Lampert, J. Diamond,W. Kaye, Controlled family study of
anorexia nervosa and bulimia nervosa: evidence of shared liability and transmission
of partial syndromes, Am. J. Psychiatry 157 (2000) 393–401.
[11] K.L. Klump, Puberty as a critical risk period for eating disorders: a review of human
and animal studies, Horm. Behav. 64 (2013) 399–410.
[12] M. Atiye, J. Miettunen, A. Raevuori-Helkamaa, A meta-analysis of temperament in
eating disorders, Eur. Eat. Disord. Rev. 23 (2015) 89–99.
[13] O. Kampman, M. Viikki, K. Jarventausta, E. Leinonen, Meta-analysis of anxiety disorders
and temperament, Neuropsychobiology 69 (2014) 175–186.
[14] F.J. Gazendam, J.H. Kamphuis, M. Kindt, Deficient safety learning characterizes high
trait anxious individuals, Biol. Psychol. 92 (2013) 342–352.
[15] E. Glotzbach-Schoon, R. Tadda,M. Andreatta, C. Troger, H. Ewald, C. Grillon, P. Pauli,
A. Muhlberger, Enhanced discrimination between threatening and safe contexts in
high-anxious individuals, Biol. Psychol. 93 (2013) 159–166.
[16] I. Indovina, T.W. Robbins, A.O. Nunez-Elizalde, B.D. Dunn, S.J. Bishop, Fearconditioningmechanisms
associated with trait vulnerability to anxiety in humans,
Neuron 69 (2011) 563–571.
[17] P. Duits, D.C. Cath, S. Lissek, J.J. Hox, A.O. Hamm, I.M. Engelhard,M.A. van den Hout,
J.M. Baas, Updatedmeta-analysis of classical fear conditioning in the anxiety disorders,
Depress. Anxiety 32 (4) (2015) 239–253.
[18] M. Strober, Pathologic fear conditioning and anorexia nervosa: on the search for
novel paradigms, Int. J. Eat. Disord. 35 (2004) 504–508.
[19] J. Lock, G.D. Le, W.S. Agras, A. Moye, S.W. Bryson, B. Jo, Randomized clinical trial
comparing family-based treatment with adolescent-focused individual therapy
for adolescents with anorexia nervosa, Arch. Gen. Psychiatry 67 (2010)
1025–1032.
[20] J. Lock, An update on evidence-based psychosocial treatments for eating disorders
in children and adolescents, J. Clin. Child Adolesc. Psychol. (2015) 1–15.
[21] APA, Practice guideline for the treatment of patients with eating disorders (revision):
American Psychiatric Association Work Group on Eating Disorders, Am. J.
Psychiatry 157 (1 Suppl.) (2000) 1–39.
[22] NICE, National Institute for Clinical Excellence (NICE) Clinical Guideline 9 Eating
Disorders, Developed by the National Collaborating Center for Mental Health, UK
2004, pp. 1–36.
[23] C.V. Wiseman, S.R. Sunday, F. Klapper, W.A. Harris, K.A. Halmi, Changing patterns
of hospitalization in eating disorder patients, Int. J. Eat. Disord. 30 (2001) 69–74.
[24] S.A. Baran, T.E. Weltzin,W.H. Kaye, Low discharge weight and outcome in anorexia
nervosa, Am. J. Psychiatry 152 (1995) 1070–1072.
[25] D. Rigaud, H. Pennacchio, C. Bizeul, V. Reveillard, B. Verges, Outcome in AN adult
patients: a 13-year follow-up in 484 patients, DiabetesMetab. 37 (2011) 305–311.
[26] A.S. Kaplan, B.T. Walsh, M. Olmsted, E. Attia, J.C. Carter, M.J. Devlin, K.M. Pike, B.
Woodside, W. Rockert, C.A. Roberto, M. Parides, The slippery slope: prediction of successful
weight maintenance in anorexia nervosa, Psychol. Med. 39 (2009) 1037–1045.
[27] G.W. Redgrave, J.W. Coughlin, C.C. Schreyer, L.M.Martin, A.K. Leonpacher,M. Seide,
A.M. Verdi, A. Pletch, A.S. Guarda, Refeeding and weight restoration outcomes in
anorexia nervosa: challenging current guidelines, Int. J. Eat. Disord. (2015)
https://dx.doi.org/10.1002/eat.22390.
[28] J.C. Carter, E. Blackmore, K. Sutandar-Pinnock, D.B. Woodside, Relapse in anorexia
nervosa: a survival analysis, Psychol. Med. 34 (2004) 671–679.
[29] J.C. Carter, K.B. Mercer-Lynn, S.J. Norwood, C.V. Bewell-Weiss, R.D. Crosby, D.B.
Woodside, M.P. Olmsted, A prospective study of predictors of relapse in anorexia
nervosa: implications for relapse prevention, Psychiatry Res. 200 (2012) 518–523.
[30] B.T. Walsh, The enigmatic persistence of anorexia nervosa, Am. J. Psychiatry 170
(2013) 477–484.
[31] J.E. Schebendach, L.E. Mayer, M.J. Devlin, E. Attia, I.R. Contento, R.L. Wolf, B.T.
Walsh, Food choice and diet variety in weight-restored patients with anorexia
nervosa, J. Am. Diet. Assoc. 111 (2011) 732–736.
[32] J.E. Dellava, L.M. Thornton, R.M. Hamer, M. Strober, K. Plotnicov, K.L. Klump, H.
Brandt, S. Crawford, M.M. Fichter, K.A. Halmi, I. Jones, C. Johnson, A.S. Kaplan, M.
Lavia, J. Mitchell, A. Rotondo, J. Treasure, D.B. Woodside, W.H. Berrettini, W.H.
Kaye, C.M. Bulik, Childhood anxiety associated with low BMI in women with anorexia
nervosa, Behav. Res. Ther. 48 (2010) 60–67.
[33] T.J. Raney, L.M. Thornton, W. Berrettini, H. Brandt, S. Crawford, M.M. Fichter,
K.A. Halmi, C. Johnson, A.S. Kaplan, M. Lavia, J. Mitchell, A. Rotondo, M.
Strober, D.B. Woodside, W.H. Kaye, C.M. Bulik, Influence of overanxious disorder
of childhood on the expression of anorexia nervosa, Int. J. Eat. Disord. 41
(2008) 326–332.
[34] W.H. Kaye, C.M. Bulik, L. Thornton, N. Barbarich, K.Masters, Comorbidity of anxiety
disorders with anorexia and bulimia nervosa, Am. J. Psychiatry 161 (2004)
2215–2221.
[35] C.A. Levinson, T.L. Rodebaugh, E.K. White, A.R. Menatti, J.W. Weeks, J.M. Iacovino,
C.S. Warren, Social appearance anxiety, perfectionism, and fear of negative evaluation:
distinct or shared risk factors for social anxiety and eating disorders? Appetite
67 (2013) 125–133.
[36] M.J. Jacobs, S. Roesch, S.A. Wonderlich, R. Crosby, L. Thornton, D.E. Wilfley, W.H.
Berrettini, H. Brandt, S. Crawford, M.M. Fichter, K.A. Halmi, C. Johnson, A.S.
Kaplan, M. Lavia, J.E. Mitchell, A. Rotondo, M. Strober, D.B. Woodside, W.H. Kaye,
C.M. Bulik, Anorexia nervosa trios: behavioral profiles of individuals with anorexia
nervosa and their parents, Psychol. Med. 39 (2009) 451–461.
[37] A. Keyes, J. Borzek, A. Henschel, O. Mickelsen, H.L. Taylor, The Biology of Human
Starvation, University of Minnesota Press, Minneapolis, 1950.
[38] L. Mattar,M.R. Thiebaud, C. Huas, C. Cebula, N. Godart, Depression, anxiety and obsessive–
compulsive symptoms in relation to nutritional status and outcome in severe
anorexia nervosa, Psychiatry Res. 200 (2012) 513–517.
[39] C. Pollice,W.H. Kaye, C.G. Greeno, T.E. Weltzin, Relationship of depression, anxiety,
and obsessionality to state of illness in anorexia nervosa, Int. J. Eat. Disord. 21
(1997) 367–376.
[40] S.E. Cassin, K.M. von Ranson, Personality and eating disorders: a decade in review,
Clin. Psychol. Rev. 25 (2005) 895–916.
[41] K.L. Klump, M. Strober, C.M. Bulik, L. Thornton, C. Johnson, B. Devlin, M.M. Fichter,
K.A. Halmi, A.S. Kaplan, D.B. Woodside, S. Crow, J. Mitchell, A. Rotondo, P.K. Keel,
W.H. Berrettini, K. Plotnicov, C. Pollice, L.R. Lilenfeld,W.H. Kaye, Personality characteristics
ofwomen before and after recovery froman eating disorder, Psychol.Med.
34 (2004) 1407–1418.
[42] K. Holtkamp, B. Muller, N. Heussen, H. Remschmidt, B. Herpertz-Dahlmann, Depression,
anxiety, and obsessionality in long-term recovered patients with adolescentonset
anorexia nervosa, Eur. Child Adolesc. Psychiatry 14 (2005) 106–110.
[43] S. Zerwas, B.C. Lund, H.A. Von, L.M. Thornton, W.H. Berrettini, H. Brandt, S.
Crawford, M.M. Fichter, K.A. Halmi, C. Johnson, A.S. Kaplan, V.M. La, J. Mitchell, A.
Rotondo, M. Strober, D.B. Woodside, W.H. Kaye, C.M. Bulik, Factors associated
with recovery from anorexia nervosa, J. Psychiatr. Res. 47 (2013) 972–979.
[44] A.S. Guarda, Treatment of anorexia nervosa: insights and obstacles, Physiol. Behav.
94 (2008) 113–120.
[45] B.J. Everitt, T.W. Robbins, Neural systems of reinforcement for drug addiction: from
actions to habits to compulsion, Nat. Neurosci. 8 (2005) 1481–1489.
[46] A.L. Milton, B.J. Everitt, The persistence of maladaptive memory: addiction, drug memories
and anti-relapse treatments, Neurosci. Biobehav. Rev. 36 (2012) 1119–1139.
[47] A. Gasbarri, A. Pompili, M.G. Packard, C. Tomaz, Habit learning andmemory inmammals:
behavioral and neural characteristics, Neurobiol. Learn. Mem. 114 (2014)
198–208.
[48] L. Rojo, L. Conesa, O. Bermudez, L. Livianos, Influence of stress in the onset of eating
disorders: data from a two-stage epidemiologic controlled study, Psychosom.Med.
68 (2006) 628–635.
[49] L. Schwabe, A. Dickinson, O.T. Wolf, Stress, habits, and drug addiction: a
psychoneuroendocrinological perspective, Exp. Clin. Psychopharmacol. 19 (2011)
53–63.
[50] S.B. Taylor, J.M. Anglin, P.R. Paode, A.G. Riggert, M.F. Olive, C.D. Conrad, Chronic
stress may facilitate the recruitment of habit- and addiction-related
neurocircuitries through neuronal restructuring of the striatum, Neuroscience
280 (2014) 231–242.
[51] T. Klengel, D. Mehta, C. Anacker, M. Rex-Haffner, J.C. Pruessner, C.M. Pariante, T.W.
Pace, K.B. Mercer, H.S. Mayberg, B. Bradley, C.B. Nemeroff, F. Holsboer, C.M. Heim,
K.J. Ressler, T. Rein, E.B. Binder, Allele-specific FKBP5 DNA demethylation mediates
gene-childhood trauma interactions, Nat. Neurosci. 16 (2013) 33–41.
[52] I. Shibuya, S. Nagamitsu, H. Okamura, H. Komatsu, S. Ozono, Y. Yamashita, T.
Matsuishi, Changes in salivary cortisol levels as a prognostic predictor in children
with anorexia nervosa, Int. J. Psychophysiol. 82 (2011) 196–201.
[53] A. Oskis, C. Loveday, F. Hucklebridge, L. Thorn, A. Clow, Diurnal patterns of salivary
cortisol and DHEA in adolescent anorexia nervosa, Stress 15 (2012) 601–607.
[54] P.Monteleone, P. Scognamiglio, A.M.Monteleone, D. Mastromo, L. Steardo Jr., I. Serino,
M. Maj, Abnormal diurnal patterns of salivary alpha-amylase and cortisol secretion in
acute patients with anorexia nervosa, World J. Biol. Psychiatry 12 (2011) 455–461.
[55] M.J. Weiser, C.D. Foradori, R.J. Handa, Estrogen receptor beta activation prevents
glucocorticoid receptor-dependent effects of the central nucleus of the amygdala
on behavior and neuroendocrine function, Brain Res. 1336 (2010) 78–88.
[56] E.A. Phelps, M.R. Delgado, K.I. Nearing, J.E. Ledoux, Extinction learning in humans:
role of the amygdala and vmPFC, Neuron 43 (2004) 897–905.
[57] M.A. Zeidan, S.A. Igoe, C. Linnman, A. Vitalo, J.B. Levine, A. Klibanski, J.M. Goldstein,
M.R. Milad, Estradiol modulates medial prefrontal cortex and amygdala activity during
fear extinction in women and female rats, Biol. Psychiatry 70 (2011) 920–927.
[58] M.C.Riddle,M.C.McKenna, Y.J. Yoon, S.S. Pattwell,P.M.Santos, B.J. Casey, C.E. Glatt, Caloric
restriction enhances fear extinction learning inmice, Neuropsychopharmacology
38 (2013) 930–937.
[59] F. Soliman, C.E. Glatt, K.G. Bath, L. Levita, R.M. Jones, S.S. Pattwell, D. Jing, N.
Tottenham, D. Amso, L.H. Somerville, H.U. Voss, G. Glover, D.J. Ballon, C. Liston, T.
Teslovich, K.T. Van, F.S. Lee, B.J. Casey, A genetic variant BDNF polymorphismalters
extinction learning in both mouse and human, Science 327 (2010) 863–866.
[60] B. Vervliet, M.G. Craske, D. Hermans, Fear extinction and relapse: state of the art,
Annu. Rev. Clin. Psychol. 9 (2013) 215–248.
[61] L.M. Shin, I. Liberzon, The neurocircuitry of fear, stress, and anxiety disorders,
Neuropsychopharmacology 35 (2010) 169–191.
[62] B.M. Graham,M.R. Milad, The study of fear extinction: implications for anxiety disorders,
Am. J. Psychiatry 168 (2011) 1255–1265.
[63] M.B. VanElzakker, M.K. Dahlgren, F.C. Davis, S. Dubois, L.M. Shin, From Pavlov to
PTSD: the extinction of conditioned fear in rodents, humans, and anxiety disorders,
Neurobiol. Learn. Mem. 113 (2014) 3–18.
[64] M.R. Milad, S.C. Furtak, J.L. Greenberg, A. Keshaviah, J.J. Im, M.J. Falkenstein, M.
Jenike, S.L. Rauch, S. Wilhelm, Deficits in conditioned fear extinction in obsessive–
compulsive disorder and neurobiological changes in the fear circuit, JAMA
Psychiatry 70 (2013) 608–618.
[65] D. Torrents-Rodas,M.A. Fullana, A. Bonillo, X. Caseras, O. Andion, R. Torrubia, No effect
of trait anxiety on differential fear conditioning or fear generalization, Biol.
Psychol. 92 (2013) 185–190.
[66] K.P. Kinzig, S.L. Hargrave, Adolescent activity-based anorexia increases anxiety-like
behavior in adulthood, Physiol. Behav. 101 (2010) 269–276.
[67] D.A. Klein, B.T. Walsh, Translational approaches to understanding anorexia
nervosa, Int. J. Eat. Disord. 37 (Suppl.) (2005) S10–S14.
[68] E. Gutierrez, A rat in the labyrinth of anorexia nervosa: contributions of the
activity-based anorexia rodent model to the understanding of anorexia nervosa,
Int. J. Eat. Disord. 46 (2013) 289–301.
[69] E. Pjetri, H.R. de, J.S. de, C. Gelegen, H. Oppelaar, L.A. Verhagen,M.J. Eijkemans, R.A.
Adan, B. Olivier,M.J. Kas, Identifying predictors of activity based anorexia susceptibility
in diverse genetic rodent populations, PLoS One 7 (2012) e50453.
[70] O. Carrera, A. Fraga, R. Pellon, E. Gutierrez, Rodent model of activity-based anorexia,
Curr. Protoc. Neurosci. 67 (2014) 9.
[71] C. Davis, S.H. Kennedy, E. Ravelski, M. Dionne, The role of physical activity in the
development and maintenance of eating disorders, Psychol. Med. 24 (1994)
957–967.
[72] L. Kron, J.L. Katz, G. Gorzynski, H. Weiner, Hyperactivity in anorexia nervosa: a fundamental
clinical feature, Compr. Psychiatry 19 (1978) 433–440.
[73] W.W. Gull, Anorexia nervosa (apepsia hysterica, anorexia hysterica)1868 Obes.
Res. 5 (1997) 498–502.
[74] C. Davis, S. Kaptein, Anorexia nervosa with excessive exercise: a phenotype with
close links to obsessive–compulsive disorder, Psychiatry Res. 142 (2006) 209–217.
[75] R. Dalle Grave, S. Calugi, G. Marchesini, Compulsive exercise to control shape or
weight in eating disorders: prevalence, associated features, and treatment outcome,
Compr. Psychiatry 49 (2008) 346–352.
[76] H. Shroff, L. Reba, L.M. Thornton, F. Tozzi, K.L. Klump,W.H. Berrettini, H. Brandt, S.
Crawford, S. Crow, M.M. Fichter, D. Goldman, K.A. Halmi, C. Johnson, A.S. Kaplan, P.
Keel, M. Lavia, J. Mitchell, A. Rotondo, M. Strober, J. Treasure, D.B. Woodside, W.H.
Kaye, C.M. Bulik, Features associatedwith excessive exercise in women with eating
disorders, Int. J. Eat. Disord. 39 (2006) 454–461.
[77] S.Young,P.Rhodes, S. Touyz, P.Hay, The relationshipbetweenobsessive–compulsive
personality disorder traits, obsessive–compulsive disorder and excessive exercise in
patients with anorexia nervosa: a systematic review, J. Eat. Disord. 1 (2013) 16.
[78] B.N. Greenwood, A.B. Loughridge, N. Sadaoui, J.P. Christianson, M. Fleshner, The
protective effects of voluntary exercise against the behavioral consequences of uncontrollable
stress persist despite an increase in anxiety following forced cessation
of exercise, Behav. Brain Res. 233 (2012) 314–321.
[79] D.A. Klein, L.E. Mayer, J.E. Schebendach, B.T.Walsh, Physical activity and cortisol in
anorexia nervosa, Psychoneuroendocrinology 32 (2007) 539–547.
[80] C.E. de Rijke, J.J. Hillebrand, L.A. Verhagen, T.A. Roeling, R.A. Adan, Hypothalamic
neuropeptide expression following chronic food restriction in sedentary and
wheel-running rats, J. Mol. Endocrinol. 35 (2005) 381–390.
[81] T.D. Muller, M. Focker, K. Holtkamp, B. Herpertz-Dahlmann, J. Hebebrand, Leptinmediated
neuroendocrine alterations in anorexia nervosa: somatic and behavioral
implications, Child Adolesc. Psychiatr. Clin. N. Am. 18 (2009) 117–129.
[82] L.A. Verhagen, M.C. Luijendijk, R.A. Adan, Leptin reduces hyperactivity in an
animal model for anorexia nervosa via the ventral tegmental area, Eur.
Neuropsychopharmacol. 21 (2011) 274–281.
[83] K.E. Giel, S. Kullmann, H. Preissl, S.C. Bischoff, A. Thiel, U. Schmidt, S. Zipfel, M.
Teufel, Understanding the reward system functioning in anorexia nervosa: crucial
role of physical activity, Biol. Psychol. 94 (2013) 575–581.
[84] W. Wang, S.L. Liu, K. Li, Y. Chen, B. Jiang, Y.K. Li, J.L. Xiao, S. Yang, T. Chen, J.G. Chen,
J.G. Li, F. Wang, Leptin: a potential anxiolytic by facilitation of fear extinction, CNS
Neurosci. Ther. (2015) https://dx.doi.org/10.1111/cns.12375.
[85] Z. Haque, N. Akbar, F. Yasmin, M.A. Haleem, D.J. Haleem, Inhibition of immobilization
stress-induced anorexia, behavioral deficits, and plasma corticosterone secretion
by injected leptin in rats, Stress 16 (2013) 353–362.
[86] N.C. Liang, N.T. Bello, T.H. Moran, Experience with activity based anorexia
enhances conditioned taste aversion learning in rats, Physiol. Behav. 102
(2011) 51–57.
[87] C. Boyd, S. Abraham, J. Kellow, Psychological features are important predictors of
functional gastrointestinal disorders in patients with eating disorders, Scand. J.
Gastroenterol. 40 (2005) 929–935.
[88] A. Icenhour, J. Langhorst, S. Benson, M. Schlamann, S. Hampel, H. Engler, M.
Forsting, S. Elsenbruch, Neural circuitry of abdominal pain-related fear learning
and reinstatement in irritable bowel syndrome, Neurogastroenterol. Motil. 27
(2015) 114–127.
[89] L.A. Eckel, The ovarian hormone estradiol plays a crucial role in the control of food
intake in females, Physiol. Behav. 104 (2011) 517–524.
[90] L.M. Jappe, L. Cao, R.D. Crosby, S.J. Crow, C.B. Peterson, G.D. Le, S.G. Engel, S.A.
Wonderlich, Stress and eating disorder behavior in anorexia nervosa as a function
of menstrual cycle status, Int. J. Eat. Disord. 47 (2014) 181–188.
[91] M. Misra, D.K. Katzman, N.M. Estella, K.T. Eddy, T. Weigel, M.A. Goldstein, K.K.
Miller, A. Klibanski, Impact of physiologic estrogen replacement on anxiety symptoms,
body shape perception, and eating attitudes in adolescent girls with anorexia
nervosa: data from a randomized controlled trial, J. Clin. Psychiatry 74 (2013)
e765–e771.
[92] N. Lagunas, I. Calmarza-Font, Y. Diz-Chaves, L.M. Garcia-Segura, Long-termovariectomy
enhances anxiety and depressive-like behaviors in mice submitted to chronic
unpredictable stress, Horm. Behav. 58 (2010) 786–791.
[93] G.D. Petrovich, M.A. Lougee, Sex differences in fear-induced feeding cessation:
prolonged effect in female rats, Physiol. Behav. 104 (2011) 996–1001.
[94] G.D. Petrovich, Forebrain networks and the control of feeding by environmental
learned cues, Physiol. Behav. 121 (2013) 10–18.
[95] K. Lebron-Milad, M.R. Milad, Sex differences, gonadal hormones and the fear extinction
network: implications for anxiety disorders, Biol. Mood Anxiety Disord.
2 (2012) 3.
[96] M.R.Milad, S.A. Igoe, K. Lebron-Milad, J.E. Novales, Estrous cycle phase and gonadal
hormones influence conditioned fear extinction, Neuroscience 164 (2009)
887–895.
[97] K.K. Cover, L.Y. Maeng, K. Lebron-Milad, M.R. Milad, Mechanisms of estradiol in
fear circuitry: implications for sex differences in psychopathology, Transl. Psychiatry
4 (2014) e422.
[98] E.M. Glover, T. Jovanovic, K.B. Mercer, K. Kerley, B. Bradley, K.J. Ressler, S.D.
Norrholm, Estrogen levels are associated with extinction deficits in women with
posttraumatic stress disorder, Biol. Psychiatry 72 (2012) 19–24.
[99] D.R. Mishell Jr., I.H. Thorneycroft, R.M. Nakamura, Y. Nagata, S.C. Stone, Serum estradiol
in women ingesting combination oral contraceptive steroids, Am. J. Obstet.
Gynecol. 114 (1972) 923–928.
[100] B.M. Graham, M.R. Milad, Blockade of estrogen by hormonal contraceptives impairs
fear extinction in female rats and women, Biol. Psychiatry 73 (2013)
371–378.
[101] J.E. Steinglass, R. Sysko, L. Mayer, L.A. Berner, J. Schebendach, Y. Wang, H. Chen,
A.M. Albano, H.B. Simpson, B.T.Walsh, Pre-meal anxiety and food intake in anorexia
nervosa, Appetite 55 (2010) 214–218.
[102] J.E. Steinglass, A.M. Albano, H.B. Simpson, Y. Wang, J. Zou, E. Attia, B.T. Walsh,
Confronting fear using exposure and response prevention for anorexia nervosa:
A randomized controlled pilot study, Int. J. Eat. Disord. 47 (2014) 174–180.
[103] K. Baek, J.H. Chae, J. Jeong, The effect of repetitive transcranialmagnetic stimulation
on fear extinction in rats, Neuroscience 200 (2012) 159–165.
[104] T. Hildebrandt, T. Bacow, M. Markella, K.L. Loeb, Anxiety in anorexia nervosa and
its management using family-based treatment, Eur. Eat. Disord. Rev. 20 (1)
(2010) e1–e16.
[105] C. Stiles-Shields, R.R. Hoste, P.M. Doyle, G.D. Le, A reviewof family-based treatment
for adolescents with eating disorders, Rev. Recent Clin. Trials 7 (2012) 133–140.
[106] A.S. Guarda, C.S. Schreyer, J.W. Coughlin, Treatment resistance: persuasion, perceived
coercion and compulsion, in: I.F. Dancyger, V.M. Fornari (Eds.), Evidence
Based Treatments for Eating Disorders, 2nd ed.Nova Science Publishers, Inc.
2014, pp. 219–235.
[107] A. Koskina, I.C. Campbell, U. Schmidt, Exposure therapy in eating disorders
revisited, Neurosci. Biobehav. Rev. 37 (2013) 193–208.
[108] H. Rodrigues, I. Figueira, A. Lopes, R. Goncalves, M.V. Mendlowicz, E.S. Coutinho, P.
Ventura, Does D-cycloserine enhance exposure therapy for anxiety disorders in
humans? A meta-analysis, PLoS One 9 (2014) e93519.
[109] J. Steinglass, R. Sysko, J. Schebendach, A. Broft, M. Strober, B.T. Walsh, The application
of exposure therapy and D-cycloserine to the treatment of anorexia nervosa: a
preliminary trial, J. Psychiatr. Pract. 13 (2007) 238–245.
[110] J.E. Steinglass, S.C. Kaplan, Y. Liu, Y.Wang, B.T.Walsh, The (lack of) effect of alprazolam
on eating behavior in anorexia nervosa: a preliminary report, Int. J. Eat.
Disord. 47 (2014) 901–904.
[111] M.S. George, H.E. Ward Jr., P.T. Ninan, M. Pollack, Z. Nahas, B. Anderson, S. Kose,
R.H. Howland,W.K. Goodman, J.C. Ballenger, A pilot study of vagus nerve stimulation
(VNS) for treatment-resistant anxiety disorders, Brain Stimul. 1 (2008)
112–121.
[112] D.F. Pena, N.D. Engineer, C.K. McIntyre, Rapid remission of conditioned fear expression
with extinction training paired with vagus nerve stimulation, Biol. Psychiatry
73 (2013) 1071–1077.
[113] D.F. Pena, J.E. Childs, S.Willett, A. Vital, C.K. McIntyre, S. Kroener, Vagus nerve stimulation
enhances extinction of conditioned fear and modulates plasticity in the
pathway from the ventromedial prefrontal cortex to the amygdala, Front. Behav.
Neurosci. 8 (2014) 327.
[114] A. Guhn, T. Dresler, M. Andreatta, L.D. Muller, T. Hahn, S.V. Tupak, T. Polak, J.
Deckert, M.J. Herrmann, Medial prefrontal cortex stimulation modulates the processing
of conditioned fear, Front. Behav. Neurosci. 8 (2014) 44.